ホワイトバイオテクノロジー 2025-2035技術、予測、市場、プレーヤーWhite Biotechnology 2025-2035: Technologies, Forecasts, Markets, Players 化学・素材用途の工業用バイオ製造。工業的発酵プロセス35以上のバイオ製造分子に関する技術分析と展望。バイオ製造の市場評価と10年間の市場予測 ホワイトバイオテクノロジーバイオエコノミー... もっと見る

サマリー
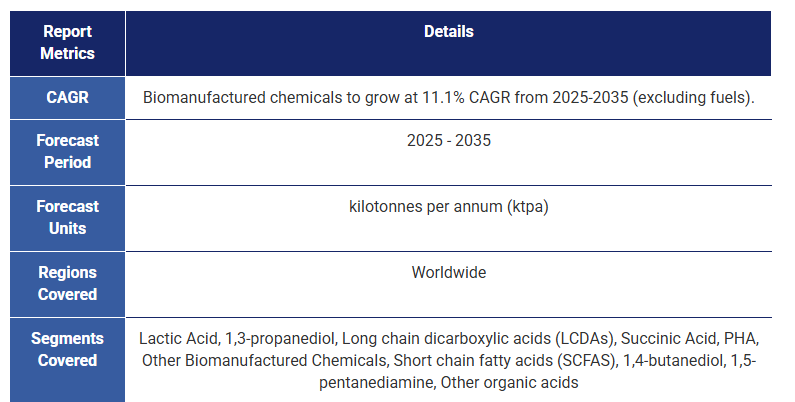
化学・素材用途の工業用バイオ製造。工業的発酵プロセス35以上のバイオ製造分子に関する技術分析と展望。バイオ製造の市場評価と10年間の市場予測
ホワイトバイオテクノロジーバイオエコノミーの推進
バイオエコノミーは、社会が再生可能な生物資源(陸上、漁業、養殖環境由来など)を利用して、食品や栄養素、化学物質や材料、バイオエネルギーなどのバイオベース製品を生み出す経済システムと定義できる。バイオエコノミーの発展は、より循環型の持続可能な経済を創造する上で重要な側面であり、化石燃料資源への世界的な依存によって気候変動の影響が悪化している現在、特に重要な課題である。
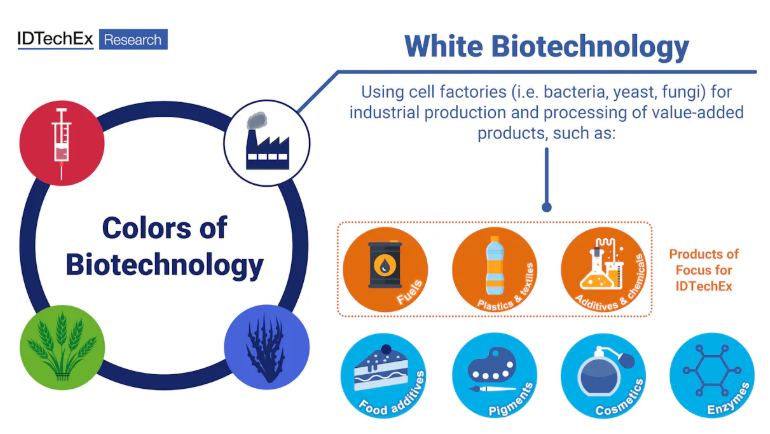
バイオテクノロジーのさまざまな分野(または「色」)によって、経済のさまざまな分野を積極的に改善することができるため、バイオテクノロジーの進歩はバイオエコノミーの拡大にとって極めて重要である。例えば、"グリーン "バイオテクノロジーは農産物の収量を向上させるために使われ、"レッド "バイオテクノロジーは新しいワクチンの製造に応用される。バイオテクノロジーのスペクトルの数ある色の中でも、ホワイト・バイオテクノロジーは、生物学的システムを通じてバイオベース製品の工業生産を促進することで、バイオエコノミーを実現する重要な技術として際立っている。
本レポート「ホワイトバイオテクノロジー 2025-2035」において、IDTechExはホワイトバイオテクノロジーの現状を独自に分析し、技術革新と歴史的、現在的、将来的なプロジェクトを批判的に考察することで、ホワイトバイオテクノロジーの将来についての客観的な評価を提供している。
ホワイトバイオテクノロジーとは何か?
工業的バイオ製造と呼ばれることもあるホワイト・バイオテクノロジーとは、バクテリア、酵母、菌類などの生きた細胞工場を使って、化学物質、材料、エネルギーを工業的に生産・加工することである。ホワイト・バイオテクノロジーは、石油ベースの化学生産に代わる、より持続可能な選択肢のひとつである。化石燃料への社会の依存を減らすだけでなく、より少ないエネルギーで、より少ない廃棄物を生み出し、潜在的に環境に優しい生分解性製品を生み出すものである。

ホワイト・バイオテクノロジーは特に新しいものではない。1980年代から洗剤用の人工酵素がホワイト・バイオテクノロジーによって製造されてきたし、細菌酵素は何年も前から食品添加物として使用されてきた。では、なぜ今ホワイトバイオテクノロジーが注目されているのだろうか?
IDTechExは本レポートの中で、ホワイトバイオテクノロジーの成長と関連性の高まりを牽引する技術革新に光を当てている。バイオテクノロジーのツールやプロセスの改良に伴い、ホワイトバイオテクノロジーによって汎用化学品から高機能繊維に至るまで、数多くの重要な製品を生産できるようになった。主要な技術ドライバーの1つは合成生物学であり、産業や研究への応用を改善する目的で生物学的システムや生物を人工的に設計・工学化することである。IDTechExは、合成生物学のツールや技術、アプリケーション、新興プレーヤーなどを考察することで、産業用バイオ製造における合成生物学の重要性について広範な議論を提供している。IDTechExは、ホワイトバイオテクノロジーを可能にする技術の進歩に関する分析を続け、他のトレンドの中でも特に以下のものについて詳細な調査(ステータス、技術的な利点と課題、商業活動を含む)を行っている:
工業的バイオ製造からのバイオベース製品:多様なスペクトル
ホワイトバイオテクノロジーを向上させるイノベーションと同様に重要なのは、その応用、すなわち人工細胞工場の発酵によって生産される化学物質、前駆物質、添加剤、および材料である。バイオ製造が可能な分子や化合物の範囲は、潤滑油から皮革、繊維製品から包装、接着剤から添加剤など、あらゆる分野での使用例があり、驚くほど多様である。これらの分子には、アルコール、ジオール、ジアミン、有機酸、タンパク質などが含まれる。
IDTechExでは、このようなホワイトバイオテクノロジーの数多くの製品を明確にするため、40以上のバイオ製造分子について詳細な技術・市場分析を行い、以下のような各分子の必須要因に注目している:
IDTechExのこれらの洞察により、ホワイトバイオテクノロジー産業の現状と成長する多用途性を明確に理解することができる。
乳酸:
本レポートで取り上げている数多くのバイオベース分子の中でも、ポリ乳酸(PLA)の需要増に大きく牽引され、急速に重要性を増している乳酸は際立っている。乳酸由来の生分解性ポリマーであるPLAは、パッケージングや消費財において、従来の化石由来プラスチックの代替品として勢いを増している。この需要急増は、環境規制の強化、特に非生分解性プラスチックへの規制が堆肥化可能な代替品への国家的な後押しに拍車をかけている中国での規制強化が顕著に影響している。その結果、国内外のPLAメーカーが生産能力を拡大し、乳酸サプライチェーンの並行成長に拍車をかけている。
ホワイト・バイオテクノロジーにおけるAIの影響
人工知能(AI)は、ホワイト・バイオテクノロジーの開発と最適化において極めて重要な存在になりつつある。菌株工学を加速することで、AIアルゴリズムはゲノムと代謝のデータセットを分析し、微生物細胞工場における収量、耐性、生産性の向上のための最適な遺伝子組み換えを予測することができる。バイオプロセス開発では、機械学習モデルを用いて発酵条件をイン・シリコで最適化し、コストと時間のかかる実験室での試験の必要性を減らしている。AIはまた、産業利用のための候補分子を迅速にスクリーニングすることで、酵素発見やタンパク質工学においても重要な役割を果たしている。ホワイトバイオテクノロジーがその応用範囲を拡大し続ける中、AIの統合はプロセスの効率性、拡張性、費用対効果を劇的に改善し、従来の石油化学生産に代わる持続可能な選択肢としてのこの分野の価値提案を強化することになる。
ホワイトバイオテクノロジー:
ホワイトバイオテクノロジーによって生産される分子の多様なスペクトルに伴い、工業的バイオ製造活動を推進しようとする多数の企業が存在する。IDTechExは本レポートの中で、多国籍材料・化学コングロマリットから新興の新興企業まで、ホワイトバイオテクノロジーへの取り組みを追求する100社を超える企業について考察している。パートナーシップ、資金調達、過去のプロジェクト、追求中の分子、現在の生産能力などの重要な情報は、これほど多くの企業がホワイトバイオテクノロジーに取り組むことを選択した方法と理由を理解するために強調されている。これらの情報は、IDTechExによるこの市場の主要プレーヤーのインタビューベースの企業プロフィールによって強化される。
ホワイトバイオテクノロジーのプレーヤー事情は、産業バイオ製造業を形成している全体的な市場ダイナミクスの一要素に過ぎない。特定のホワイトバイオテクノロジープロジェクトの経済的実行可能性を決定するためには、プロセス収率、規模の拡大容易性、バイオ触媒の選択などの内部要因から、政府規制、原油価格、グリーンプレミアムなどの外部要因に至るまで、評価すべき数多くの要因が存在する。本レポートでは、こうした観点からホワイトバイオテクノロジー市場を分析し、業界のこれまでの軌跡を理解するとともに、将来の成功を左右する要因についての洞察を提供する。
主要分子別にセグメント化したホワイトバイオテクノロジー10年市場予測
最後に、ホワイトバイオテクノロジー産業の成長可能性を特定するため、IDTechExは世界の生産能力に基づいて主要バイオ製造分子10種類別に市場をセグメント化した産業バイオ製造予測を提供している。本レポートでは、各セグメントにおける現在の生産能力、促進要因、制約に注目し、それらを10年予測に外挿することで、成熟したホワイトバイオテクノロジー製品と新興のホワイトバイオテクノロジー製品、技術準備、破壊の可能性、ホワイトバイオテクノロジーの将来の展望を探っている。
主要な側面
目次
1.要旨
1.1.用語集
1.2.バイオテクノロジーの色
1.3.ホワイトバイオテクノロジーとは?
1.4.ホワイトバイオテクノロジー2025-2035:範囲
1.5.ホワイトバイオテクノロジーの動向と推進要因
1.6.ホワイトバイオテクノロジーに応用される合成生物学
1.7.ホワイトバイオテクノロジーの技術動向
1.8.ホワイトバイオテクノロジーの代替原料の概要
1.9.ホワイトバイオテクノロジーに関する主な市場課題
1.10.ホワイトバイオテクノロジーが直面する技術的課題
1.11.ホワイトバイオテクノロジーに由来する製品概要
1.12.工業的バイオ製造によって生産できる分子
1.13.工業的バイオ製造によって生産できる分子
1.14.ホワイトバイオテクノロジーにおける企業展望
1.15.ホワイトバイオテクノロジーにおける企業展望
1.16.ホワイトバイオテクノロジーによる次世代燃料
1.17.ホワイトバイオテクノロジーによるバイオプラスチック
1.18.単糖類からのバイオベースポリマー
1.19.ホワイトバイオテクノロジーで合成される一般的なバイオプラスチックとポリマー前駆体
1.20.ホワイトバイオテクノロジーで生産される分子の現状
1.21.ホワイトバイオテクノロジーの分子別市場シェア 2025-2035
1.22.ホワイトバイオテクノロジー世界生産能力予測 2025-2035 1.23.ホワイトバイオテクノロジー世界生産能力予測 2025-2035
1.23:考察(I)
1.24.白色バイオテクノロジー世界生産能力予測 2025-2035年
1.24:考察(Ⅱ)
1.25.ホワイトバイオテクノロジーの新興分野 2025-2035年予測
1.26.IDTechExの循環型バイオエコノミー研究
1.27.企業プロファイル
1.28.IDTechEx サブスクリプションでさらにアクセス
2.はじめに
2.1.略語集
2.2.略語集
2.3.用語集
2.4.用語集
2.5.バイオテクノロジーの色
2.6.白いバイオテクノロジーとは
2.7.バイオエコノミーとホワイトバイオテクノロジー
2.8.ホワイトバイオテクノロジー2025-2035:範囲
3.市場分析
3.1.ホワイトバイオテクノロジーの市場促進要因
3.1.1.市場推進要因:バイオベース製品に対する需要
3.1.2.市場促進要因石油由来プラスチック使用に対する政府の規制
3.1.3.市場促進要因:バイオマニュファクチャリング需要に影響を与えそうな規制
3.1.4.市場の推進要因:規制により中国では生分解性プラスチックへの関心が高まっている
3.1.5.市場の推進要因:バイオテクノロジーに対する政府の支援
3.1.6.市場の推進要因:バイオテクノロジーに対する政府の支援
3.1.7.市場促進要因:炭素税 3.2.ホワイトバイオテクノロジーの経済的実行可能性
3.2.1.ホワイト・バイオテクノロジー・プロジェクトの経済的実行可能性に影響を与える要因
3.2.2.ブレント原油価格がバイオベース製品に及ぼす影響
3.2.3.グリーン・プレミアム
3.2.4.原料価格の上昇
3.2.5.細胞工場のコストへの影響
3.2.6.価格から見たバイオベース化の可能性が最も高い化学物質の特定
3.2.7.スケールアップがコストに与える影響
3.2.8.ザイマーゲン社:合成生物学の経済性に関するケーススタディ
3.2.9.ケーススタディランザテック
3.2.10.ケーススタディソラザイム社
3.2.11.合成生物学:汎用製品から少量高価値市場へのシフト
3.2.12.ホワイトバイオテクノロジーにとっての主な市場課題
3.3.プレーヤー、新興企業、地域の状況
3.3.1.バイオ製造による化学品の地域別生産能力 2025年
3.3.2.地域別分析:地域別分析:バイオマニュファクチャリングの地域別生産と需要の推進要因と阻害要因 3.3.3.地域別分析:研究開発拠点と生産拠点
3.3.4.地域別分析:バイオマニュファクチャリング
3.3.5.地域別分析:地域別生産能力
3.3.6.プレーヤー:合成生物学ツールとプラットフォーム
3.3.7.プレーヤー垂直統合型バイオマニュファクチャリング
3.3.8.分子別にセグメント化された新興プレーヤー
3.3.9.分子別にみた新興プレーヤー
3.3.10.ホワイトバイオテクノロジーに関わる化学・素材企業の概要
3.3.11.ホワイトバイオテクノロジーに関わる化学・素材企業の概要
4.ホワイトバイオテクノロジー用細胞工場
4.1.バイオ製造のための細胞工場:考慮すべき要因
4.2.バイオ製造のための細胞工場:様々な生物
4.3.大腸菌(E.coli)
4.4.コリネバクテリウム・グルタミカム(C. glutamicum)
4.5.枯草菌(B. subtilis)
4.6.サッカロマイセス・セレビシエ(S. cerevisiae)
4.7.ヤロウィア・リポリティカ(Y. lipolytica)
4.8.様々なバイオ製造プロセスで使用される微生物
4.9.ホワイトバイオテクノロジーの非モデル生物
5.技術開発
5.1.合成生物学
5.1.1.合成生物学:生物システムの設計と工学
5.1.2.合成生物学:セントラルドグマの操作
5.1.3.合成生物学の広大な範囲
5.1.4.合成生物学のプロセス:設計、構築、試験
5.1.5.合成生物学:なぜ今なのか
5.1.6.合成生物学:医薬品から消費者製品へ
5.1.7.合成生物学:既存のサプライチェーンを破壊する
5.1.8.合成生物学:導入の推進要因と障壁
5.1.9.ホワイトバイオテクノロジーに応用される合成生物学
5.2.合成生物学のツールと技術
5.2.1.合成生物学のツールと技術概要
5.2.2.DNA合成
5.2.3.CRISPR-Cas9の紹介
5.2.4.CRISPR-Cas9:細菌の免疫システム
5.2.5.合成生物学におけるCRISPR-Cas9の重要性
5.2.6.タンパク質/酵素工学
5.2.7.コンピュータ支援設計
5.2.8.工業的応用における工学的タンパク質の商業的例
5.2.9.株の構築と最適化
5.2.10.合成生物学と代謝工学の相乗効果
5.2.11.産業用微生物株開発のフレームワーク
5.2.12.規模の問題
5.2.13.無細胞システムの紹介
5.2.14.無細胞系と細胞系システム
5.2.15.ホワイトバイオテクノロジーにおける無細胞システム
5.2.16.ホワイトバイオテクノロジーにおける無細胞システム
5.2.17.無細胞システムの商業的導入:Solugen
5.2.18.ホワイトバイオのための無細胞システムを追求する新興企業
5.2.19.ホワイトバイオテクノロジーで無細胞システムを追求する新興企業
5.2.20.ホワイトバイオテクノロジーにおける固定化酵素
5.2.21.ホワイトバイオテクノロジーにおける固定化触媒
5.2.22.ロボット工学:ハンズフリーでハイスループットの科学を可能にする
5.2.23.ロボットによるクラウドラボラトリー
5.2.24.生物設計の自動化とループの閉鎖
5.2.25.人工知能と機械学習
5.2.26.機械学習によるde novoタンパク質予測
5.2.27.バイオ製造における機械学習による改善の概要
5.2.28.AI主導の発酵プラットフォーム企業
5.3.バイオ製造プロセスの改善
5.3.1.連続バイオ製造とバッチバイオ製造
5.3.2.連続バイオ製造の利点と課題
5.3.3.連続バイオ製造とバッチバイオ製造:主要発酵パラメーターの比較
5.3.4.機械学習によるバイオ製造プロセスの改善
5.3.5.ダウンストリーム処理(DSP)の改善
5.3.6.下流工程(DSP)の改善(2)
5.3.7.灌流バイオリアクター
5.3.8.下流バイオプロセスにおけるタンジェンシャルフローろ過(TFF)
5.3.9.バイオテクノロジーと化学のハイブリッドアプローチ
5.3.10.プロセス強化および高セル密度発酵
5.4.持続可能性のためのホワイトバイオテクノロジー
5.4.1.持続可能な技術としてのホワイトバイオテクノロジー
5.4.2.ホワイトバイオテクノロジーにおける炭素捕獲のルート
5.4.3.バイオ製造による炭素回収のための独立栄養細菌
5.5.バイオ製造のための代替原料
5.5.1.なぜホワイトバイオテクノロジーに代替原料を使うのか
5.5.2.食糧、土地、水の競合
5.5.3.C1原料:代謝経路
5.5.4.C1原料:経済的利益
5.5.5.C1原料:課題
5.5.6.非メタンC1原料
5.5.7.C1原料製品
5.5.8.C1原料ガス発酵
5.5.9.C2原料
5.5.10.C2原料原料別に区分された製品
5.5.11.C1およびC2原料:商業活動
5.5.12.C1およびC2原料:商業活動
5.5.13.リグノセルロース系バイオマス原料
5.5.14.リグノセルロース系バイオマス原料:課題
5.5.15.リグノセルロース系バイオマス原料:課題
5.5.16.リグノセルロース系バイオマス原料:製品
5.5.17.リグノセルロース系バイオマス原料:製品
5.5.18.リグノセルロース系バイオマス原料:商業活動
6.ブルーバイオテクノロジー
6.1.ブルーバイオテクノロジーとは何か
6.2.ブルーバイオテクノロジーの主な生体触媒:シアノバクテリアと藻類
6.3.シアノバクテリア
6.4.藻類
6.5.ブルーバイオテクノロジーの主要推進要因と課題
6.6.ブルーバイオテクノロジーにおける主な新興企業
7.ホワイトバイオテクノロジーに由来する製品
7.1.1.ホワイトバイオテクノロジー由来の製品:概要
7.2.燃料
7.2.1.バイオ燃料世代 - 従来型バイオ燃料と先進バイオ燃料
7.2.2.バイオ燃料の世代
7.2.3.ホワイトバイオテクノロジーによるバイオ燃料
7.2.4.バイオ燃料への代謝経路
7.2.5.バイオエタノール
7.2.6.次世代バイオエタノール
7.2.7.次世代バイオエタノール:障壁
7.2.8.次世代エタノール - 運転プラント
7.2.9.次世代エタノール - 運転プラント
7.2.10.次世代エタノール - 運転プラント
7.2.11.次世代エタノール-操業プラント
7.2.12.次世代エタノール-操業中プラント
7.2.13.次世代エタノール計画プラント
7.2.14.次世代エタノール計画プラント
7.2.15.次世代エタノール-非稼働・中止プラント
7.2.16.次世代エタノール-非稼働および中止プラント
7.2.17.バイオ製造経路からのディーゼル
7.2.18.ファルネセン
7.2.19. n-ブタノール
7.2.20.イソブタノール
7.2.21.メタノール
7.2.22.バイオ燃料生産におけるブルーバイオテクノロジー
7.2.23.バイオディーゼル生産におけるブルーバイオテクノロジー
7.2.24.バイオエタノール生産におけるブルーバイオテクノロジー
7.2.25.バイオ燃料生産におけるブルーバイオテクノロジー:商業的実現に向けた主要課題
7.2.26.バイオ燃料生産のためのブルーバイオテクノロジー:米国の石油生産業者による商業活動
7.2.27.バイオ燃料生産のためのブルーバイオテクノロジー:米国以外の石油生産者による商業活動
7.2.28.バイオ燃料生産のためのブルーバイオテクノロジー:現在および過去のプレーヤー一覧
7.2.29.バイオ燃料生産のためのブルーバイオテクノロジー:現・旧プレーヤーのリスト
7.2.30.バイオ燃料生産のためのブルーバイオテクノロジー: 7.3.プラスチックと繊維
7.3.1.バイオプラスチックの紹介
7.3.2.ホワイトバイオテクノロジーによるバイオプラスチックの生産
7.3.3.単糖類からのバイオベースポリマーの開発
7.3.4.ホワイトバイオテクノロジーによって合成される一般的なバイオプラスチックとポリマー前駆体
7.3.5.乳酸とポリ乳酸(PLA)
7.3.6.乳酸(C3H6O3)
7.3.7.乳酸:細菌発酵か化学合成か
7.3.8.発酵に最適な乳酸菌株
7.3.9.乳酸発酵のための酵母株工学
7.3.10.発酵、回収、精製
7.3.11.ポリ乳酸とは
7.3.12.ポリ乳酸の製造
7.3.13.ポリ乳酸の製造工程
7.3.14.ポリ乳酸:SWOT分析
7.3.15.その他のバイオベース合成ポリエステルの分子
7.3.16.バイオ製造モノマーから得られるバイオベースポリエステルの範囲
7.3.17.プロピレングリコール(PG)または1,2-プロパンジオール
7.3.18.1,3-プロパンジオール(1,3-PDO)
7.3.19.バイオベースのPDOとPTT:モノマー製造
7.3.20.バイオベースPDOとPTT:ポリマー用途
7.3.21. 2,3-ブタンジオール(2,3-BDO)
7.3.22.1,4-ブタンジオール(1,4-BDO)
7.3.23.バイオベースBDO:モノマー製造
7.3.24.ジェノ社からライセンス供与されたバイオベースBDO技術
7.3.25.バイオベースBDOとPBT:ポリマー用途
7.3.26.コハク酸
7.3.27.バイオベースのコハク酸モノマー製造
7.3.28.バイオベースコハク酸とPBS:ポリマーへの応用
7.3.29.バイオベースコハク酸プロジェクトの現状
7.3.30.2,5-フランジカルボン酸(FDCA)
7.3.31.バイオベースFDCA:モノマー生産
7.3.32.ポリエチレンフラノエート(PEF)
7.3.33.バイオベースFDCAとPEF:ポリマーへの応用
7.3.34.その他のバイオベース合成ポリマーのための分子
7.3.35.ポリアミドへの生合成経路
7.3.36.C6:アジピン酸、ヘキサメチレンジアミン、カプロラクタム
7.3.37.C10:セバシン酸
7.3.38.C12:ドデカン二酸
7.3.39.1,5-ペンタンジアミン(PDA)
7.3.40.コベストロPDIおよびDesmodur eco脂肪族ポリイソシアネート
7.3.41.キャセイ・インダストリアル・バイオテック: TERRYL および ECOPENT バイオベースポリアミド 7.3.42.1,3-ブタジエン
7.3.43.バイオ製造由来のブタジエン・プロジェクトの現状
7.3.44.イソプレン
7.3.45.イソブテン(イソブチレン)
7.3.46.天然由来のバイオベースポリマー:ポリヒドロキシアルカノエート(PHA)
7.3.47.ポリヒドロキシアルカノエートの紹介
7.3.48.PHAの生合成経路
7.3.49.発酵、回収、精製
7.3.50.主な市販PHAと微細構造
7.3.51.PHB、PHBV、P(3HB-co-4HB)
7.3.52.PHAの種類
7.3.53.市販のPHAの材料特性
7.3.54.PHAのサプライヤー
7.3.55.短鎖と中鎖のPHA
7.3.56.PHA:SWOT分析
7.3.57.PHAの応用
7.3.58.PHAのビジネスチャンス
7.3.59.PHA製造コストの削減
7.3.60.PHAのリスク
7.3.61.PHAは少量しか製造されない
7.3.62.PHA製造施設
7.3.63.ケーススタディダニマー・サイエンティフィック社、PHA生産を終了
7.3.64.結論
7.3.65.ホワイトバイオテクノロジーで生産されるその他の繊維
7.3.66.クモの糸
7.3.67.コラーゲン由来の繊維製品
7.3.68.菌糸
7.4.その他の化学物質、前駆体、添加物
7.4.1.アセトン
7.4.2.アクリル酸
7.4.3.アセトン
7.4.4.イタコン酸
7.4.5.前駆体としてのバイオベースエタノール
7.4.6.エチレンのバイオ製造
7.4.7.モノエチレングリコール(MEG)
7.4.8.バイオベースMEG:モノマー生産
7.4.9.バイオベースMEG:産業展望
7.4.10.バイオベースMEG:産業展望
7.4.11.ポリエチレンテレフタレート(PET)
7.4.12.バイオベース・ポリオレフィン
7.4.13.ブラスケン:「私は環境に優しい」ポリエチレン
7.4.14.プロピレン前駆体のバイオ製造
7.4.15.マロン酸
7.4.16.短鎖脂肪酸と中鎖脂肪酸(SCFA/MCFA)
7.4.17.短鎖脂肪酸と中鎖脂肪酸(SCFA/MCFA)
7.4.18.短鎖脂肪酸:酢酸
7.4.19.トリグリセリド
7.4.20.その他の有機酸とアルデヒド
7.4.21.その他の有機酸とアルデヒド
7.4.22.バクテリアセルロース
7.5.ホワイトバイオテクノロジーに由来するその他の製品
7.5.1.ホワイトバイオテクノロジーで生産されるビタミンとアミノ酸の概要
7.5.2.化粧品用ホワイトバイオテクノロジーの概要
7.5.3.界面活性剤と洗剤のバイオ製造
7.5.4.オンワード用の酵素ノボザイムズ
7.5.5.バイオ製造によるセメント代替品:バイオメイソン
7.5.6.精密発酵:定義と範囲
8.白色バイオテクノロジーの予測
8.1.予測方法
8.2.分子別ホワイトバイオテクノロジー市場シェア 2025-2035
8.3.ホワイトバイオテクノロジーの世界生産能力予測 2025-2035
8.4.白色バイオテクノロジー世界生産能力予測 2025-2035:考察(I)
8.5.白色バイオテクノロジー世界生産能力予測 2025-2035:考察
8.6.白色バイオテクノロジー世界生産能力予測 2025-2035年考察
8.7.2025~2035年のホワイトバイオテクノロジー新興分野予測
8.8.ホワイトバイオテクノロジーの新興分野予測考察
9.企業プロファイル
9.1.アフィレン
9.2.アルゼダ
9.3.バイオメーソン
9.4.ボルトスレッド
9.5.ブラスケン
9.6.キャセイバイオテック
9.7.カーボンブリッジ
9.8.セルティック・リニューアブルズ
9.9.チェーンクラフト
9.10.シアノキャプチャー
9.11.エコバティブ
9.12.Enginzyme
9.13.エンザイマスター
9.14.工業用微生物
9.15.クレイグ・バイオクラフト研究所
9.16.ランザテック(2023年)最新情報
9.17.ランザテック
9.18.マンゴーマテリアル
9.19.モダン・メドウ
9.20.ニューエナジーブルー
9.21.ノボザイムズ
9.22.Qパワー
9.23.スパイバー
9.24.河南徳光バイオテクノロジー
9.25.Huitong Biomaterials
9.26.トータルエナジー・コルビオン
9.27.帝人フロンティアPLA
9.28.ネイチャーワークス
9.29.バイオティック・サーキュラー・テクノロジーズ
9.30.ブルーファ
9.31.CJバイオマテリアルズ
9.32.ダニマー・サイエンティフィック(2024年最新情報-現在は倒産)
9.33.ダニマー・サイエンティフィック
9.34.フォータム:INGAプラスチック
9.35.カネカ
9.36.ニューライト・テクノロジーズ(現在は操業していない)
9.37.オウロビオ
9.38.Paques Biomaterials
10.付録
10.1.ホワイトバイオテクノロジーの世界生産能力予測 2025-2035
10.2.ホワイトバイオテクノロジーの新興分野 2025-2035年予測
Summary
Industrial biomanufacturing for chemicals and materials applications. Industrial fermentation processes. Technology analysis and outlook for 35+ biomanufactured molecules. Biomanufacturing market appraisal and 10-year market forecast.
White biotechnology: Advancing the bioeconomy
The bioeconomy can be defined as an economic system in which society uses renewable biological resources (i.e. derived from land, fisheries, and aquaculture environments) to create biobased products such as food and nutrients, chemicals and materials, and bio-energy. Developing the bioeconomy is a key aspect of creating a more circular sustainable economy, an especially critical task as the effects of climate change are exacerbated by global reliance on fossil fuel resources.
The advancement of biotechnology is critical to expanding the bioeconomy, as different areas (or "colors") of biotechnology can positively improve different sectors of the economy. For example, "green" biotechnology may be used to improve agricultural yields, while "red" biotechnology may be applied towards the creation of new vaccines. Of the numerous colors of the biotechnology spectrum, white biotechnology stands out as a key technology enabler for the bioeconomy by advancing the industrial production of biobased products through biological systems.
In this report, "White Biotechnology 2025-2035", IDTechEx provides independent analysis of the status of white biotechnology, looking critically at technology innovations and historic, current, and future projects to provide an objective assessment of white biotechnology's future.
What is white biotechnology, and why does it matter?
White biotechnology, sometimes called industrial biomanufacturing, is the industrial production and processing of chemicals, materials, and energy using living cell factories, like bacteria, yeast, and fungi. White biotechnology represents a more sustainable alternative to petroleum-based chemical production: one that not only decreases society's reliance on fossil fuels but also uses less energy, generates less waste, and potentially creates biodegradable products that are better for the environment.

White biotechnology is not particularly new; engineered enzymes for detergents have been produced via white biotechnology since the 1980s, and bacterial enzymes have been used as food additives for many, many years. That begs the question: why is white biotechnology so interesting now?
IDTechEx, in this report, sheds light on the technology innovations driving white biotechnology's growth and increasing relevance. With improvements in biotechnology tools and processes comes the ability to produce numerous important products, from commodity chemicals to high performance textiles, through white biotechnology. One main technology driver is synthetic biology - the artificial design and engineering of biological systems and living organisms for the purpose of improving applications for industry or research. IDTechEx offers extensive discussion on synthetic biology's importance to industrial biomanufacturing by considering synthetic biology's tools and techniques, applications, emerging players, etc. IDTechEx continues their analysis of the technology advances enabling white biotechnology with detailed examinations (including status, technical benefits and challenges, commercial activity), among other trends, of:
Biobased products from industrial biomanufacturing: a diverse spectrum
Just as important as the innovations improving white biotechnology are its applications - the chemicals, precursors, additives, and materials produced by the fermentation of engineered cell factories. The range of molecules and compounds that can be biomanufactured is incredibly diverse with use cases in everything from lubricants to leather, textiles to packaging, adhesives to additives, etc. These molecules include alcohols, diols, diamines, organic acids, proteins, and more.
To provide clarity on these many products of white biotechnology, IDTechEx provides detailed technical and market analysis on 40+ biomanufactured molecules, looking at essential factors for each molecule such as:
With these IDTechEx insights, a clear understanding of the status and growing versatility of the white biotechnology industry will be achieved.
Lactic acid: Experiencing accelerating growth through regulation-driven PLA demand
Among the many biobased molecules covered in this report, lactic acid stands out for its rapidly growing significance, driven largely by increased demand for polylactic acid (PLA). PLA, a biodegradable polymer derived from lactic acid, is gaining momentum as a substitute for traditional fossil-based plastics in packaging and consumer goods. This surge in demand is notably influenced by tightening environmental regulations, particularly in China, where restrictions on non-biodegradable plastics have spurred a national push toward compostable alternatives. As a result, both domestic and international PLA producers are scaling up production capacity, fueling parallel growth in the lactic acid supply chain.
The Impact of AI on White Biotechnology
Artificial intelligence (AI) is increasingly becoming a pivotal enabler in the development and optimization of white biotechnology. By accelerating strain engineering, AI algorithms can analyze genomic and metabolic datasets to predict optimal genetic modifications for improved yield, tolerance, or productivity in microbial cell factories. In bioprocess development, machine learning models are being used to optimize fermentation conditions in silico, reducing the need for costly and time-consuming laboratory trials. AI also plays a vital role in enzyme discovery and protein engineering by rapidly screening candidate molecules for industrial use. As white biotechnology continues to expand its application scope, the integration of AI stands to dramatically improve process efficiency, scalability, and cost effectiveness, reinforcing the field's value proposition as a sustainable alternative to traditional petrochemical production.
White biotechnology: An active market of established and emerging players
With the diverse spectrum of molecules being produced through white biotechnology, there is a large number of companies attempting to advance their industrial biomanufacturing activities. Within this report, IDTechEx has considered well over 100 companies pursuing white biotechnology efforts, ranging from multinational material and chemical conglomerates to nascent startups. Important information such as partnerships, funding, past projects, molecules being pursued, current production capacity, and more are highlighted to understand how and why so many companies have chosen to engage with white biotechnology. These will be bolstered by IDTechEx's interview-based company profiles of key players in this market.
The player landscape of white biotechnology is just one component of the overall market dynamics that are shaping industrial biomanufacturing. There are numerous factors to be evaluated to determine the economic viability of certain white biotechnology projects, from internal factors such as process yield, ease of scale, and biocatalyst choice to external factors such as government regulations, crude oil prices, and the green premium. This report analyzes the white biotechnology market from these perspectives to offer understanding on the industry's prior trajectory and insight on what will determine its future success.
White biotechnology 10-year market forecast segmented by major molecules
Lastly, to identify the growth potential of the white biotechnology industry, IDTechEx provides industrial biomanufacturing forecasts that segments the market by ten major biomanufactured molecules based on global production capacity. The report looks at the current capacity, drivers, and constraints of each segment and then extrapolates them into a 10-year forecast, to explore the mature and emerging white biotechnology products, technology readiness, potential for disruption, and the future landscape of white biotechnology.
Key Aspects:
Table of Contents1. EXECUTIVE SUMMARY
1.1. Glossary of terms
1.2. Colors of biotechnology
1.3. What is white biotechnology?
1.4. White Biotechnology 2025-2035: scope
1.5. Trends and drivers in white biotechnology
1.6. Synthetic biology as applied to white biotechnology
1.7. Technology trends in white biotechnology
1.8. Overview of alternative feedstocks for white biotechnology
1.9. Major market challenges for white biotechnology
1.10. Technical challenges facing white biotechnology
1.11. Products derived from white biotechnology: Overview
1.12. Molecules that can be produced through industrial biomanufacturing
1.13. Molecules that can be produced through industrial biomanufacturing
1.14. Company landscape in white biotechnology
1.15. Company landscape in white biotechnology
1.16. Next-generation fuels through white biotechnology
1.17. Bioplastics through white biotechnology
1.18. Navigating biobased polymers from monosaccharides
1.19. Common bioplastics and polymer precursors synthesized via white biotechnology
1.20. Status of molecules produced through white biotechnology
1.21. White biotechnology market share by molecule 2025-2035
1.22. White biotechnology global capacity forecast 2025-2035
1.23. White biotechnology global capacity forecast 2025-2035: Discussion (I)
1.24. White biotechnology global capacity forecast 2025-2035: Discussion (II)
1.25. Emerging areas of white biotechnology forecast 2025-2035
1.26. IDTechEx circular bioeconomy research
1.27. Company profiles
1.28. Access More With an IDTechEx Subscription
2. INTRODUCTION
2.1. Glossary of acronyms
2.2. Glossary of acronyms
2.3. Glossary of terms
2.4. Glossary of terms
2.5. Colors of biotechnology
2.6. What is white biotechnology?
2.7. The bioeconomy and white biotechnology
2.8. White Biotechnology 2025-2035: Scope
3. MARKET ANALYSIS
3.1. Market Drivers for White Biotechnology
3.1.1. Market drivers: Demand for biobased products
3.1.2. Market drivers: Government regulation on petroleum-based plastic use
3.1.3. Market drivers: Regulations that are likely to impact biomanufacturing demand
3.1.4. Market drivers: Regulations are driving strong interest in biodegradable plastics in China
3.1.5. Market drivers: Government support of biotechnology
3.1.6. Market drivers: Government support of biotechnology
3.1.7. Market drivers: Carbon taxes
3.2. Economic Viability of White Biotechnology
3.2.1. Factors affecting the economic viability of white biotechnology projects
3.2.2. Effect of the price of Brent crude on biobased products
3.2.3. The Green Premium
3.2.4. Rising feedstock prices
3.2.5. Effect of cell factory on cost
3.2.6. Identifying the chemicals with the most potential to become biobased based on price
3.2.7. How scale-up affects cost
3.2.8. Zymergen: Case study on economics of synthetic biology
3.2.9. Case study: LanzaTech
3.2.10. Case study: Solazyme
3.2.11. Synthetic biology: Shift from commodity products to lower volume, high value markets
3.2.12. Major market challenges for white biotechnology
3.3. Player, Start-up, and Regional Landscape
3.3.1. Production capacity of chemicals from biomanufacturing by region 2025
3.3.2. Regional analysis: Drivers and restraints for biomanufacturing production and demand by region
3.3.3. Regional analysis: Location of R&D vs production
3.3.4. Regional analysis: Biomanufacturing
3.3.5. Regional analysis: Production capacity by region
3.3.6. Players: Synthetic biology tools and platforms
3.3.7. Players: Vertically integrated biomanufacturing
3.3.8. Emerging players segmented by molecule
3.3.9. Emerging players segmented by molecule
3.3.10. Overview of chemicals and materials companies involved with white biotechnology
3.3.11. Overview of chemicals and materials companies involved in white biotechnology
4. CELL FACTORIES FOR WHITE BIOTECHNOLOGY
4.1. Cell factories for biomanufacturing: Factors to consider
4.2. Cell factories for biomanufacturing: A range of organisms
4.3. Escherichia coli (E.coli)
4.4. Corynebacterium glutamicum (C. glutamicum)
4.5. Bacillus subtilis (B. subtilis)
4.6. Saccharomyces cerevisiae (S. cerevisiae)
4.7. Yarrowia lipolytica (Y. lipolytica)
4.8. Microorganisms used in different biomanufacturing processes
4.9. Non-model organisms for white biotechnology
5. TECHNOLOGY DEVELOPMENTS
5.1. Synthetic Biology
5.1.1. Synthetic biology: The design and engineering of biological systems
5.1.2. Synthetic biology: Manipulating the central dogma
5.1.3. The vast scope of synthetic biology
5.1.4. The process of synthetic biology: Design, build and test
5.1.5. Synthetic biology: Why now?
5.1.6. Synthetic biology: From pharmaceuticals to consumer products
5.1.7. Synthetic biology: Disrupting existing supply chains
5.1.8. Synthetic biology: Drivers and barriers for adoption
5.1.9. Synthetic biology as applied to white biotechnology
5.2. Tools and Techniques of Synthetic Biology
5.2.1. Tools and techniques of synthetic biology: Overview
5.2.2. DNA synthesis
5.2.3. Introduction to CRISPR-Cas9
5.2.4. CRISPR-Cas9: A bacterial immune system
5.2.5. CRISPR-Cas9's importance to synthetic biology
5.2.6. Protein/enzyme engineering
5.2.7. Computer-aided design
5.2.8. Commercial examples of engineered proteins in industrial applications
5.2.9. Strain construction and optimization
5.2.10. Synergy between synthetic biology and metabolic engineering
5.2.11. Framework for developing industrial microbial strains
5.2.12. The problem with scale
5.2.13. Introduction to cell-free systems
5.2.14. Cell-free versus cell-based systems
5.2.15. Cell-free systems in the context of white biotechnology
5.2.16. Cell-free systems for white biotechnology
5.2.17. Commercial implementation of cell-free systems: Solugen
5.2.18. Startups pursuing cell-free systems for white biotechnology
5.2.19. Startups pursuing cell-free systems for white biotechnology
5.2.20. Immobilized enzymes in white biotechnology
5.2.21. Immobilized catalysts in white biotechnology
5.2.22. Robotics: enabling hands-free and high throughput science
5.2.23. Robotic cloud laboratories
5.2.24. Automating organism design and closing the loop
5.2.25. Artificial intelligence and machine learning
5.2.26. Machine learning de novo protein prediction
5.2.27. Overview of machine learning based improvements for biomanufacturing
5.2.28. AI-driven fermentation platform companies
5.3. Improvement of Biomanufacturing Processes
5.3.1. Continuous vs batch biomanufacturing
5.3.2. Benefits and challenges of continuous biomanufacturing
5.3.3. Continuous vs batch biomanufacturing: Key fermentation parameter comparison
5.3.4. Machine learning to improve biomanufacturing processes
5.3.5. Downstream processing (DSP) improvements
5.3.6. Downstream processing (DSP) improvements (2)
5.3.7. Perfusion bioreactors
5.3.8. Tangential flow filtration (TFF) in downstream bioprocessing
5.3.9. Hybrid biotechnological-chemical approaches
5.3.10. Process intensification and high-cell-density fermentation
5.4. White Biotechnology for Sustainability
5.4.1. White biotechnology as a sustainable technology
5.4.2. Routes for carbon capture in white biotechnology
5.4.3. Autotrophic bacteria for carbon capture through biomanufacturing
5.5. Alternative Feedstocks for Biomanufacturing
5.5.1. Why use alternative feedstocks for white biotechnology?
5.5.2. Food, land, and water competition
5.5.3. C1 feedstocks: Metabolic pathways
5.5.4. C1 feedstocks: Economic benefits
5.5.5. C1 feedstocks: Challenges
5.5.6. Non-methane C1 feedstocks
5.5.7. C1 feedstocks: Products
5.5.8. C1 feedstocks: Gas fermentation
5.5.9. C2 feedstocks
5.5.10. C2 feedstocks: Products segmented by feedstock
5.5.11. C1 and C2 feedstocks: Commercial activity
5.5.12. C1 and C2 feedstocks: Commercial activity
5.5.13. Lignocellulosic biomass feedstocks
5.5.14. Lignocellulosic biomass feedstocks: Challenges
5.5.15. Lignocellulosic biomass feedstocks: Challenges
5.5.16. Lignocellulosic biomass feedstocks: Products
5.5.17. Lignocellulosic biomass feedstocks: Products
5.5.18. Lignocellulosic feedstocks: Commercial activity
6. BLUE BIOTECHNOLOGY
6.1. What is blue biotechnology?
6.2. Main biocatalysts of blue biotechnology: Cyanobacteria and algae
6.3. Cyanobacteria
6.4. Algae
6.5. Key drivers and challenges for blue biotechnology
6.6. Selected startups in blue biotechnology
7. PRODUCTS DERIVED FROM WHITE BIOTECHNOLOGY
7.1.1. Products derived from white biotechnology: Overview
7.2. Fuels
7.2.1. Biofuel generations - conventional & advanced biofuels
7.2.2. Biofuel generations
7.2.3. Biofuels made from white biotechnology
7.2.4. Metabolic pathways to biofuels
7.2.5. Bioethanol
7.2.6. Next-generation bioethanol
7.2.7. Next generation bioethanol: Barriers
7.2.8. Next-generation ethanol - operational plants
7.2.9. Next-generation ethanol - operational plants
7.2.10. Next-generation ethanol - operational plants
7.2.11. Next-generation ethanol - operational plants
7.2.12. Next-generation ethanol - operational plants
7.2.13. Next-generation ethanol - planned plants
7.2.14. Next-generation ethanol - planned plants
7.2.15. Next-generation ethanol - non-operational and cancelled plants
7.2.16. Next-generation ethanol - non-operational and cancelled plants
7.2.17. Diesel from biomanufacturing pathways
7.2.18. Farnesene
7.2.19. n-Butanol
7.2.20. Isobutanol
7.2.21. Methanol
7.2.22. Blue biotechnology in biofuel production
7.2.23. Blue biotechnology in biodiesel production
7.2.24. Blue biotechnology in bioethanol production
7.2.25. Blue biotechnology for biofuel production: Key challenges for commercial viability
7.2.26. Blue biotechnology for biofuel production: Commercial activity by US oil producers
7.2.27. Blue biotechnology for biofuel production: Commercial activity by non-US oil producers
7.2.28. Blue biotechnology for biofuel production: List of current and former players
7.2.29. Blue biotechnology for biofuel production: List of current and former players
7.2.30. Blue biotechnology for biofuel production: List of current and former players
7.3. Plastics and Textiles
7.3.1. Introduction to bioplastics
7.3.2. Production of bioplastics through white biotechnology
7.3.3. Navigating biobased polymers from monosaccharides
7.3.4. Common bioplastics and polymer precursors synthesized via white biotechnology
7.3.5. Lactic Acid and Polylactic Acid (PLA)
7.3.6. Lactic acid (C3H6O3)
7.3.7. Lactic acid: Bacterial fermentation or chemical synthesis?
7.3.8. Optimal lactic acid bacteria strains for fermentation
7.3.9. Engineering yeast strains for lactic acid fermentation
7.3.10. Fermentation, recovery and purification
7.3.11. What is polylactic acid?
7.3.12. Production of PLA
7.3.13. PLA production process
7.3.14. Polylactic acid: A SWOT analysis
7.3.15. Molecules for Other Biobased Synthetic Polyesters
7.3.16. The range of available biobased polyesters from bio-manufactured monomers
7.3.17. Propylene glycol (PG) or 1,2-propanediol
7.3.18. 1,3-Propanediol (1,3-PDO)
7.3.19. Biobased PDO and PTT: Monomer production
7.3.20. Biobased PDO and PTT: Polymer applications
7.3.21. 2,3-Butanediol (2,3-BDO)
7.3.22. 1,4-Butanediol (1,4-BDO)
7.3.23. Biobased BDO: Monomer production
7.3.24. Biobased BDO technology licensed from Geno
7.3.25. Biobased BDO and PBT: Polymer applications
7.3.26. Succinic acid
7.3.27. Biobased succinic acid: Monomer production
7.3.28. Biobased succinic acid and PBS: Polymer applications
7.3.29. Biobased succinic acid: Project status
7.3.30. 2,5-furandicarboxylic acid (FDCA)
7.3.31. Biobased FDCA: Monomer production
7.3.32. Polyethylene furanoate (PEF)
7.3.33. Biobased FDCA and PEF: Polymer applications
7.3.34. Molecules for Other Biobased Synthetic Polymers
7.3.35. Biosynthetic pathways to polyamides
7.3.36. C6: Adipic acid, hexamethylenediamine, and caprolactam
7.3.37. C10: Sebacic acid
7.3.38. C12: Dodecanedioic acid
7.3.39. 1,5-Pentanediamine (PDA)
7.3.40. Covestro: PDI and Desmodur eco aliphatic polyisocyanate
7.3.41. Cathay Industrial Biotech: TERRYL and ECOPENT biobased polyamides
7.3.42. 1,3-Butadiene
7.3.43. Status of biomanufacturing-derived butadiene projects
7.3.44. Isoprene
7.3.45. Isobutene (isobutylene)
7.3.46. Naturally Occurring Biobased Polymers: Polyhydroxyalkanoates (PHAs)
7.3.47. Introduction to poly(hydroxyalkanoates)
7.3.48. Biosynthetic pathways to PHAs
7.3.49. Fermentation, recovery and purification
7.3.50. Key commercial PHAs and microstructures
7.3.51. PHB, PHBV, and P(3HB-co-4HB)
7.3.52. Types of PHAs
7.3.53. Material properties of commercial PHAs
7.3.54. Suppliers of PHAs
7.3.55. Short and medium chain-length PHAs
7.3.56. PHAs: A SWOT analysis
7.3.57. Applications of PHAs
7.3.58. Opportunities in PHAs
7.3.59. Reducing the cost of PHA production
7.3.60. Risks in PHAs
7.3.61. PHAs are only made in small quantities
7.3.62. PHA production facilities
7.3.63. Case Study: Danimer Scientific ends PHA production
7.3.64. Conclusions
7.3.65. Other Textiles Produced through White Biotechnology
7.3.66. Spider silk
7.3.67. Collagen-derived textiles
7.3.68. Mycelium
7.4. Other Chemicals, Precursors, and Additives
7.4.1. Acetone
7.4.2. Acrylic acid
7.4.3. Acetone
7.4.4. Itaconic acid
7.4.5. Biobased ethanol as a precursor
7.4.6. Biomanufacturing of ethylene
7.4.7. Monoethylene glycol (MEG)
7.4.8. Biobased MEG: Monomer production
7.4.9. Biobased MEG: Industry landscape
7.4.10. Biobased MEG: Industry landscape
7.4.11. Polyethylene terephthalate (PET)
7.4.12. Biobased polyolefins
7.4.13. Braskem: "I'm green" polyethylene
7.4.14. Biomanufacturing of propylene precursors
7.4.15. Malonic acid
7.4.16. Short chain fatty acids and medium chain fatty acids (SCFAs/MCFAs)
7.4.17. Short chain fatty acids and medium chain fatty acids (SCFAs/MCFAs)
7.4.18. Short chain fatty acids: Acetic acid
7.4.19. Triglycerides
7.4.20. Other organic acids and aldehydes
7.4.21. Other organic acids and aldehydes
7.4.22. Bacterial cellulose
7.5. Other Products Derived from White Biotechnology
7.5.1. Overview of vitamins and amino acids produced through white biotechnology
7.5.2. Overview of white biotechnology for cosmetics
7.5.3. Biomanufacturing for surfactants and detergents
7.5.4. Enzymes for onward use: Novozymes
7.5.5. Cement alternatives from biomanufacturing: BioMason
7.5.6. Precision fermentation: Definition and scope
8. FORECASTS FOR WHITE BIOTECHNOLOGY
8.1. Forecast methodology
8.2. White biotechnology market share by molecule 2025-2035
8.3. White biotechnology global capacity forecast 2025-2035
8.4. White biotechnology global capacity forecast 2025-2035: Discussion (I)
8.5. White biotechnology global capacity forecast 2025-2035: Discussion
8.6. White biotechnology global capacity forecast 2025-2035: Discussion
8.7. Emerging areas of white biotechnology forecast 2025-2035
8.8. Emerging areas of white biotechnology forecast: Discussion
9. COMPANY PROFILES
9.1. Afyren
9.2. Arzeda
9.3. Biomason
9.4. Bolt Threads
9.5. Braskem
9.6. Cathay Biotech
9.7. CarbonBridge
9.8. Celtic Renewables
9.9. Chaincraft
9.10. CyanoCapture
9.11. Ecovative
9.12. Enginzyme
9.13. Enzymaster
9.14. Industrial Microbes
9.15. Kraig Biocraft Laboratories
9.16. LanzaTech (2023) Update
9.17. LanzaTech
9.18. Mango Materials
9.19. Modern Meadow
9.20. New Energy Blue
9.21. Novozymes
9.22. Q Power
9.23. Spiber
9.24. Henan Techuang Biotechnology
9.25. Huitong Biomaterials
9.26. Total Energies Corbion
9.27. Teijin Frontier: PLA
9.28. Natureworks
9.29. Biotic Circular Technologies
9.30. Bluepha
9.31. CJ Biomaterials
9.32. Danimer Scientific (2024 Update - Now bankrupt)
9.33. Danimer Scientific
9.34. Fortum: INGA Plastic
9.35. Kaneka
9.36. Newlight Technologies (Not currently operational)
9.37. Ourobio
9.38. Paques Biomaterials
10. APPENDIX
10.1. White biotechnology global capacity forecast 2025-2035
10.2. Emerging areas of white biotechnology forecast 2025-2035
ご注文は、お電話またはWEBから承ります。お見積もりの作成もお気軽にご相談ください。本レポートと同分野(バイオ薬物)の最新刊レポート
IDTechEx社の バイオ薬物分野 での最新刊レポートよくあるご質問IDTechEx社はどのような調査会社ですか?IDTechExはセンサ技術や3D印刷、電気自動車などの先端技術・材料市場を対象に広範かつ詳細な調査を行っています。データリソースはIDTechExの調査レポートおよび委託調査(個別調査)を取り扱う日... もっと見る 調査レポートの納品までの日数はどの程度ですか?在庫のあるものは速納となりますが、平均的には 3-4日と見て下さい。
注文の手続きはどのようになっていますか?1)お客様からの御問い合わせをいただきます。
お支払方法の方法はどのようになっていますか?納品と同時にデータリソース社よりお客様へ請求書(必要に応じて納品書も)を発送いたします。
データリソース社はどのような会社ですか?当社は、世界各国の主要調査会社・レポート出版社と提携し、世界各国の市場調査レポートや技術動向レポートなどを日本国内の企業・公官庁及び教育研究機関に提供しております。
|
|